新聞中心
上一期小賽給大家分享了一篇KingFisher純化細胞的文章,獲得了很多小伙伴的關注,這次小賽又給您帶來了一篇KingFisher做蛋白純化的文章,KingFisher儀器不僅能用于新冠病毒的檢測,還能用于新冠藥物靶點的研究。

2020年5月,一篇名為 “A SARS-CoV-2 protein interaction map reveals targets for drug repurposing” 的重磅論文在Nature上發表,推動治療新冠藥物的研發進程。論文通過揭示SARS-CoV-2病毒與人類蛋白相互作用(protein–protein interaction, PPI)的圖譜來揭示病毒如何劫持細胞系統,找到了332個SARS-CoV-2蛋白與人類蛋白質之間的相互作用關系,并鑒定出69種能靶向干擾的化合物。這項研究無論對于“老藥新用”治療新冠疾病,還是對于指明新藥的研發方向,都有重要的意義。
值得一提的是
科學家在研究中使用了全自動純化系統KingFisher Flex (Thermo Fisher Scientific) 和質譜分析儀Q Exactive Orbitrap Mass Spectrometers (Thermo Fisher Scientific) 來實現親和純化質譜(affinity purification mass spectrometry,AP-MS),找到了藥物靶點,為新冠藥物開發助力。
研究方法
他們首先單獨研究了 29 種 SARS-CoV-2 蛋白中的 26 種(表1)。
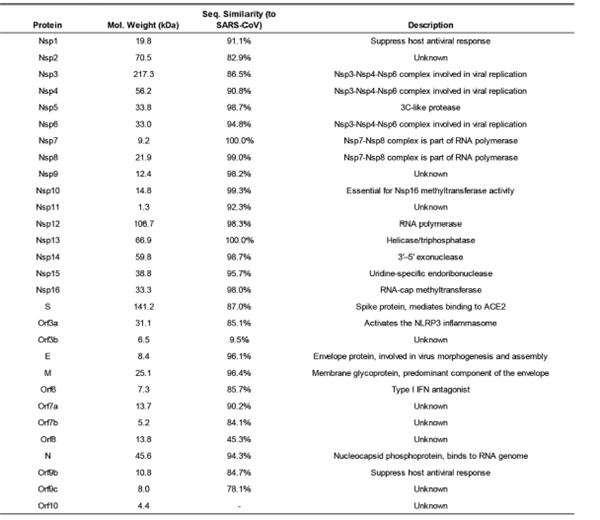
表1. SARS-CoV-2蛋白表,包括分子質量、與SARS-CoV同源物的序列相似性以及基于SARS-CoV同源物的推斷功能。
如何找到這26種病毒蛋白會與人體里的哪些蛋白產生相互作用呢?
研究人員利用在 HEK293T/17 細胞中表達的病毒蛋白進行親和純化質譜(AP-MS)。SARS-CoV-2 病毒蛋白經過密碼子優化并克隆到帶有親和標簽(或誘餌)的哺乳動物表達載體中。在宿主細胞中表達這些病毒蛋白后,通過高通量的純化系統KingFisher Flex,在與宿主蛋白相互作用的背景下純化病毒蛋白并通過多次純化洗滌,盡量避免雜蛋白的干擾。結合質譜分析得到的數據,生成SARS-CoV-2蛋白和人類蛋白之間的 PPI 圖譜(圖1)。
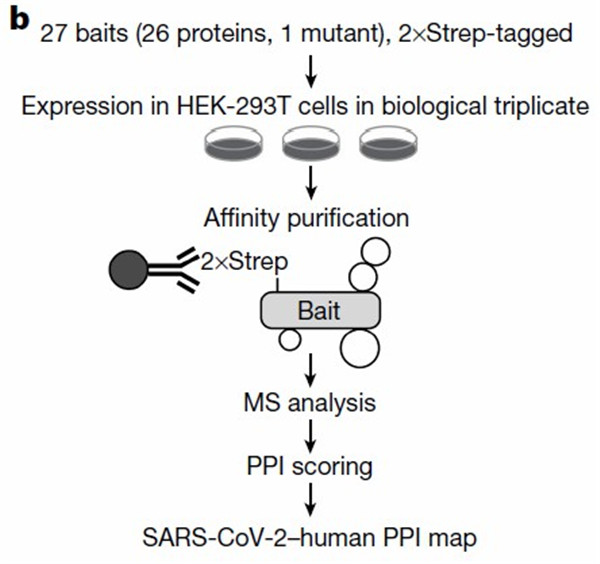
圖1. AP-MS鑒定SARS-CoV-2宿主蛋白-蛋白質相互作用的實驗流程。
根據這些蛋白相互作用的數據,科學家們在已經批準的藥物、正在臨床試驗的藥物、以及尚未進入臨床試驗的化合物中,尋找能夠選擇性干擾病毒蛋白-人類蛋白相互作用的分子。
為了進一步證明藥物的抗病毒性,研究團隊與兩個正在實驗室中處理 SARS-CoV-2 病毒的研究小組合作,在 Vero 細胞培養病毒檢測中測試病毒。
主要發現1
繪制SARS-CoV-2病毒蛋白與人體蛋白相互作用網絡
研究團隊首次系統分析了SARS-CoV-2在感染過程中可能與哪些人類蛋白質相互作用。用親和純化質譜法(AP-MS)對27個標記的病毒蛋白(26種新冠病毒蛋白和1種突變體蛋白)進行分析,基于蛋白質之間的相互作用,確定新冠蛋白與人類蛋白質的作用關系,并鑒定了332種高置信度新冠蛋白-人類蛋白相互作用網絡(圖2)。
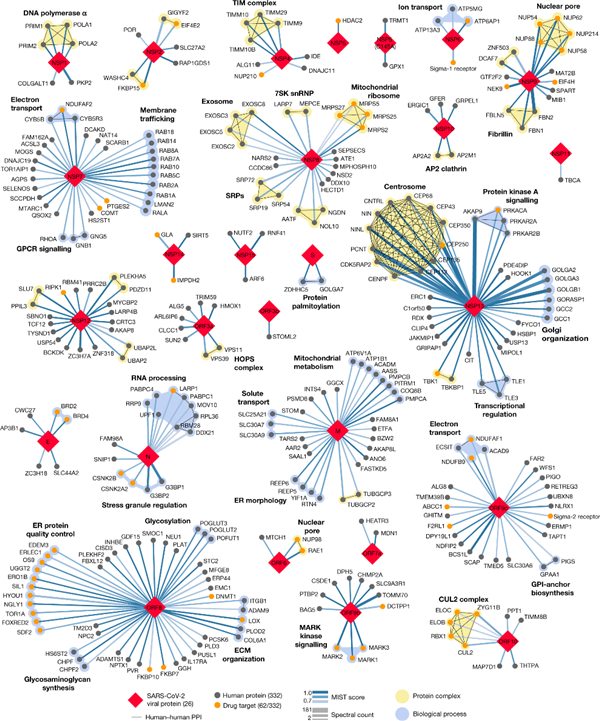
圖2. SARS-CoV-2蛋白-蛋白相互作用網絡。26種SARS-CoV-2蛋白(紅色菱形)與人類蛋白(圓形;藥物靶點:橙色;蛋白復合物:黃色;同一生物過程中的蛋白質:藍色)之間332種具有高置信度的相互作用。
為了進一步驗證互作蛋白,研究團隊研究了人類相互作用蛋白的生物學功能、解剖表達模式、SARS-CoV-2感染期間的表達變化以及與宿主-病原體相互作用蛋白的其他圖譜。科學家發現這些新冠病毒蛋白參與基因調控、信號轉導、應激反應等多個關鍵細胞進程。約40%蛋白互作蛋白與內室或者囊泡運輸途徑有關。其中新冠病毒會對多條先天免疫系統通路如干擾素通路和 NF-κB通路等產生負面影響。此外,兩個調節抗病毒先天免疫信號通路的人類蛋白,也會被新冠病毒蛋白所靶向和針對。
主要發現2
篩選干預蛋白相互作用網絡的現有藥物
通過研究蛋白互作,科學家找到了這些潛在的藥物靶點。通過整理這些會與新冠蛋白相互作用的蛋白信息,科學家們對比FDA的數據,在已經批準的藥物、正在臨床試驗的藥物、以及尚未進入臨床試驗的化合物中,找到了69個能夠選擇性干擾新冠蛋白與人類蛋白相互作用的化合物(圖3)。在這69種化合物中,27種為已經通過FDA批準上市的藥物,另外還有14種藥物目前還處于臨床研究階段,剩余28種還未進入臨床研究。

圖3. 藥物和人類靶點的網絡。圖中顯示了SARS-CoV-2毒餌與已批準藥物(綠色)、臨床候選藥物(橙色)和臨床前候選藥物(紫色)的蛋白-蛋白相互作用,以及針對宿主蛋白(白色背景)或已知宿主因子(灰色背景)的實驗活動。
是否這69種化合物都具有抗病毒活性呢?為了在體外測試這些藥物,他們在紐約和巴黎做了病毒感染性實驗(圖4)。在紐約西奈山醫院,他們開發了一種中通量免疫熒光技術分析(檢測病毒NP蛋白)篩選37種化合物,研究Vero E6細胞系SARS-CoV-2感染的抑制作用;在法國的巴斯德研究所,另一批科學家通過PCR (RT-qPCR)檢測44種藥物和化合物。這兩個實驗發現了兩類分子能減少病毒的感染性:mRNA 翻譯抑制劑和 Sigma1 和 Sigma2 受體的預測調節因子。后續研究表明,這些分子作用于病毒入侵細胞之前,可以起到阻斷病毒感染的作用。

圖4. 病毒感染性試驗示意圖。
為了理解這些抑制劑發揮抗病毒作用的機制,科學家進行了時間過程實驗,在感染前或感染后不同時間添加藥物。結果顯示(圖5)PB28、佐他替芬 (Zotatifin) 和羥基氯喹均降低了病毒的檢出,此外,這三種分子在病毒侵入后的感染后4小時內均能抑制NP的表達。因此,這些分子似乎在病毒復制過程中發揮其抗病毒作用。
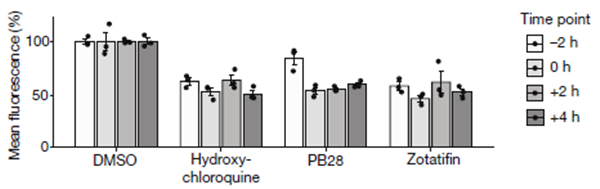
圖5. 感染前后添加藥物的抗病毒作用區別。在添加高滴度病毒(MOI = 2)之前或之后添加藥物,抗病毒效果相似。
在本研究中,KingFisher Flex幫助研究人員解決了以下問題:
1. 純化的均一性。96通量蛋白樣本在親和純化時在同一條件下完成,實驗更嚴謹。
2. 提高實驗效率。AP-MS實驗涉及大量的標簽蛋白純化,全自動純化系統KingFisher Flex代替手工操作,節約時間,可重復性強。
3. 實驗準確性。多檔速度可調搭配高吸附磁珠,實驗過程中,盡可能多的標簽蛋白被純化出來,提高藥物靶點研究的準確性。
參考文獻
David E. Gordon, Gwendolyn M. Jang, et al. A SARS-CoV-2 protein interaction map reveals targets for drug repurposing. Nature 2020, 583, 459–468
